撰文/彭梓涵(環球生技月刊記者)
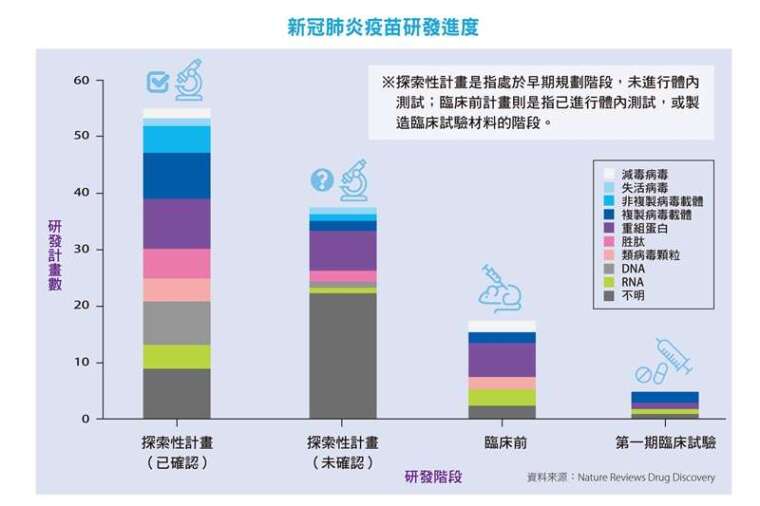
儘管東京奧運因疫情延後,另一場世界級的競技,卻在各國實驗室悄悄開打。流行病防範創新聯盟(CEPI)盤點全球新冠疫苗發展近況,截至 4 月 8 日止,全球有 115 款候選疫苗,其中 73 款已在研發與臨床前階段,5 款進入臨床。專家估計,開發一款能投入市場的疫苗,順利的話,可能需時 12 到 18 個月。
全球新冠疫苗研發競賽,領先進入臨床試驗的 5 款疫苗包括:美國 Moderna 和 Inovio Pharmaceuticals 各 1 款、中國大陸康希諾(CanSino Biologicals)1 款,以及深圳免疫基因治療研究所(Shenzhen Geno-Immune Medical Institute)的 2 款,仍是美、中藥廠捉對廝殺的局面。
其他疫苗開發商,如德國 BioNTech 與輝瑞(Pfizer)合作的 mRNA 疫苗、英國牛津大學開發的腺病毒載體疫苗,也分別在 4 月 22、23 日啟動臨床試驗;原是競爭關係的全球兩大疫苗廠賽諾菲(Sanofi)、葛蘭素史克(GlaxoSmithKline),在新冠疫情急遽升溫下,也史無前例的攜手研發,預計在今年下半年展開人體試驗。
5 款新冠疫苗進臨床 核酸疫苗靈活性大
綜觀現行疫苗開發平台,包括核酸(DNA 和 RNA)、病毒顆粒、胜肽、病毒載體、重組蛋白、以及減毒、失活病毒等。其中利用 DNA 或 mRNA 的核酸平台,在疫苗開發上展現極大靈活性,以 Moderna 的「mRNA-1273」疫苗來說,在新冠病毒序列公告後僅 2 個月,即以最快速度將疫苗推向臨床。
「mRNA-1273」疫苗之所以領先群倫,是因疫苗直接注射微脂粒包覆的 mRNA,跳過轉錄(Transcription)步驟,直接轉譯(Translation)出蛋白質,以模擬病毒感染人體的方式觸發免疫反應,開發上只要知道基因序列就可以著手製作,製備相對快速。不過,該類型疫苗易被細胞外核糖核酸酶降解,可能影響疫苗效性。
儘管至今未有相關 mRNA 疫苗獲得上市批准,但 Moderna 這款疫苗前景看好,近期 Moderna 也獲得美國政府資助 4.83 億美元,讓疫苗在進行安全性試驗的同時,立即啟動大規模疫苗生產。
4 月底啟動臨床試驗的牛津大學疫苗,目前看來頗有後發先至的潛力。英國政府提供牛津大學 2,000 萬英鎊(折合新台幣約 7.5 億元)做為疫苗研發經費,牛津團隊提取新冠病毒表面的棘蛋白基因,放入弱化的黑猩猩腺病毒中,疫苗進入人體產生棘蛋白,刺激免疫系統產生抗體,日後再接觸到新冠病毒,就有免疫能力。
牛津團隊先進行了彌猴的動物試驗,效果令人滿意,該團隊規劃下個月就要進入超過 6,000 人的試驗,一旦證明有效,最快 9 月底就可備妥百萬劑規模的疫苗。不過,疫苗與新藥研發的兩難就在於,若疫情減緩,參與試驗者的規模可能縮小到不足以驗證疫苗的有效性。

跨國聯盟推進疫苗加速開發
流行病防範創新聯盟(Coalition for Epidemic Preparedness Innovations;CEPI)是由政府、企業、學術界、慈善機構、國際組織等組成的新聯盟,於 2017 年正式成立,主要在推動、補助與協調疫苗開發,預防並控制傳染病流行。在這波疫情下,CEPI 至少資助了 4 項新冠疫苗開發計畫,前述進入臨床的 Moderna 和 Inovio Pharmaceuticals 疫苗,都是 CEPI 的注資對象。
流行病防範創新聯盟,在 3 月底於《新英格蘭醫學雜誌》(NEJM)上發表,快速開發新冠疫苗的建議,重點包括:優化抗原設計確保最佳免疫反應、挑選合適動物模型。CEPI 指出,在合適的動物模型中,進行疫苗安全性及有效性測試非常關鍵。然而,因應嚴峻疫情,快速疫苗開發應跳脫傳統開發思維,臨床前動物試驗、臨床試驗及量產應同步進行。
世界衛生組織(WHO)也在 4 月公布一份國際多疫苗株隨機試驗草案(An international randomised trial of candidate vaccines against COVID-19),又稱「團結疫苗試驗」(SOLIDARITY Vaccines Trial),將全球患者納入試驗,也讓疫情嚴重程度不同的國家,有同等試用機會,同時加速疫苗開發。目前已有 90 多個國家參與,參與國家越多,試驗結果也越快得到。
臺灣優化抗疫經驗 四大技術平台同步開發
哈佛公共衛生學院(Harvard T.H. Chan School of Public Health)專家日前發表在在《科學》(Science)期刊的一篇論文,預測在疫苗與特效藥出現前,社交距離等隔離防疫措施恐將延續到 2022 年,各國為降低防疫對經濟衝擊,對疫苗需求急切,屆時即便疫苗研發成功,也可能供不應求,成為管制出口對象。
為維持國內防疫戰力,臺灣 2 月初啟動疫苗國家隊,由國衛院領軍,同時投入胜肽、DNA、重組病毒、次單位等 4 類疫苗研發。國衛院副院長司徒惠康透露,目前進展最快的胜肽疫苗,即得力於過去 SARS 疫苗的研發成果。
「當年 SARS 爆發,國防醫學院預防醫學研究所開發出『ACE2 基因轉殖老鼠』,讓老鼠細胞表面具備人體細胞膜 ACE2 受體,」司徒惠康說,由於 SARS 與新冠病毒,都是透過 ACE2 受體進入人體,有了「ACE2 基因轉殖老鼠」,可快速試驗疫苗或藥物,無須再進口實驗動物。目前,胜肽疫苗已打入老鼠並成功產生抗體,正待確認疫苗保護力,而 DNA 疫苗也已施打老鼠並觀察免疫反應中,6 月初即可選定最佳候選疫苗。
此外,中研院生物醫學科學研究所胡哲銘團隊,以 MERS 奈米疫苗開發經驗基礎,將關鍵奈米粒子雙乳化製程技術,再次用到新冠病毒上。團隊應用水、油不相容特性,將病毒連接「蛋白質冠」接著物、蛋白質、病毒核酸、佐劑,做出具有蛋白質皇冠表面的「假病毒外殼」(Virus-Like Particles;VLPs)空包彈,透過搭載於粒子內部的強效佐劑,刺激免疫系統產生抗體,大幅提升免疫力。
利用奈米技術模仿病毒顆粒的方法,目的在於可解決傳統疫苗的侷限。例如減毒的活病毒疫苗,雖可誘發較好的免疫反應,但活病毒疫苗在製程與使用上,仍存在風險;至於死病毒疫苗,雖然病毒本身已被破壞,安全性相對好,但僅能刺激產生抗體免疫,T 細胞辨識度較差,若有少量病毒突變,容易造成免疫反應漏洞。
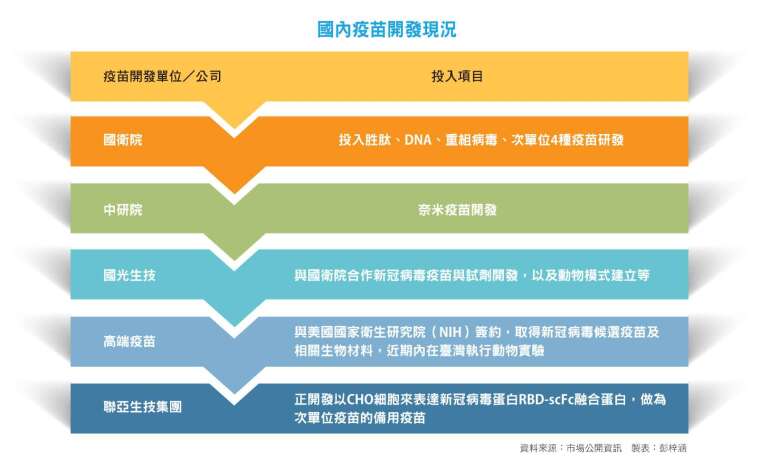
臺灣疫苗研發 國際化與產能是關鍵
除了研究機構,國內疫苗開發、生產與臨床試驗量能,還包含國光生技、高端疫苗、聯亞、台康生技、昱厚等生技業者,如何加速開發並選擇成熟且可量產的平台,也是決定臺灣今年冬天疫苗能否順利供應的關鍵因素。
疫苗研發充滿不確定性,是耐力、資源與時間的競賽,儘管臺灣疫情控制頻受國際稱許,但受限於病例樣本數少、疫苗、藥物研究的展開也相對「困難」,臺灣疫苗開發者有必要採取國際合作方式,透過病毒株或相關試驗資料交換來加快研發時程,徹底戰勝疫情。
轉載自《工業技術與資訊》月刊第 340 期 2020 年 5 月號,未經授權不得轉載。